Биология - Протеинкиназы - Тирозиновые протеинкиназы
08 февраля 2011Оглавление:
1. Протеинкиназы
2. Тирозиновые протеинкиназы
3. Серин/треонин — специфичные протеинкиназы
4. Гистидин — специфичные протеинкиназы
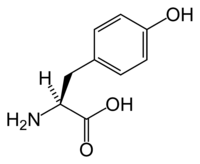
Тирозиновые протеинкиназы — ферменты, которые переносят фосфатную группу от АТФ на остаток аминокислоты тирозина в белке. Большинство тирозиновых киназ имеют сопряженные тирозинфосфатазы. Тирозиновые киназы классифицируют на две группы: цитоплазматические и трансмембранные.
Цитоплазматические протеинкиназы
Геном человека содержит 32 гена цитоплазматических тирозиновых протеинкиназ. Первым изученным геном тирозинкиназы, не связанной с рецептором, был ген из семейства Src, протоонкогенных тирозиновых киназ. Протеинкиназы этого семейства содержатся почти во всех клетках животных. Было показано, что вирус саркомы Рауса содержит мутантную копию нормального клеточного гена Src. Белки семейства Src регулируют многие процессы в клетке, участвуют в передаче интегрин-зависимых сигналов в клетку, которые побуждают её деление.
Геном ретровирусов может содержать ген v-src, который является онкогеном, он не содержит С-концевого участка, ингибирования фосфорилирования, и поэтому постоянно активен в клетке, чем отличается от c-src, которые активируется только некоторыми внешними сигналами, и является протоонкогеном.
TCR, передает сигнал внутрь клетки путем активирования двух белков Lck и Fyn, относящихся к семейству Src. Этот сигнал приводит к пролиферации Т-лимфоцитов и усилению клеточного иммунитета.
Рецепторы с тирозинкиназной активностью
Геном человека содержит 58 генов рецепторов-тирозинкиназ. Гормоны и факторы роста, которые взаимодействуют на поверхности клетки с рецепторами, обладающими тирозинкиназной акитвностью, как правило, вызывают рост клеток и стимулируют клеточные деления. Рецепторы с тирозинкиназной активностью располагаются на поверхности клеток и связывают полипептидные факторы роста, цитокины и гормоны. Такие рецепторы не только регулируют клеточные процессы, но и играют критическую роль в развитии многих видов рака.
Рецепторы с тирозинкиназной активностью по фосфорилируемому субстрату делят на двадцать семейств. Инсулиновый рецептор является мультимерным комплексом, однако большинство рецепторов с тирозинкиназной активностью имеют только одну субъединицу. Каждый мономер имеет один трансмембранный домен, состоящий из 25-38 аминокислотных остатков, внеклеточный N-концевой домен и внутриклеточный C-концевой домен. Внеклеточный домен очень крупный и отвечает за связывание лигандов, внутриклеточный участок содержит домены с киназной активностью. Когда фактор роста или гормон соединяется с внеклеточным доменом рецептора-тирозинкиназы, рецептор димеризуется. Димеризация рецепторов активирует цитоплазматические домены, которые осуществляют самофосфорилирование рецептора по многим аминокислотным остаткам.
Тирозиновые протеинкиназы принимают участие в передаче сигнала в клетке путем фосфорилирования специфических остатков тирозина белков-мишеней. Специфические белки, содержащие SH2-домены или домены связывания фосфотирозина, соединяются с рецептором и фосфорилируются внутриклеточным доменом. Фосфорилирование приводит к активации белков и инициирует пути сигнальной трансдукции. Активированные рецепторы могут взаимодействовать и с другими белками, не обладающими каталитическими активностями. Такие адапторные белки связывают рецепторы-тирозинкиназы со следующими этапами сигнальной трансдукции, например, с каскадом МАР-киназ.
Просмотров: 16141
|
|
